Představte si, že vaše tělo se stává mikroskopickou továrnou na miniaturní technologie. Zní to jako sci-fi, že? Ale co kdybych vám řekl, že vědci už teď dokáží tisknout ultrajemné struktury, včetně zmenšeného slona, přímo uvnitř živých buněk? Tento objev má potenciál změnit způsob, jakým studujeme a interagujeme s nejzákladnějšími stavebními kameny života. Není to jen teorie, je to nová realita, kterou musíte pochopit hned teď.
Proč je to pro vás důležité?
Už vás nebaví, že se všechny nové objevy zdají být pro běžného člověka nedostupné? Tato technologie otevírá dveře k preciznímu ovládání buněčných procesů a budování nástrojů pro detailnější výzkum. Myslete na to jako na novou generaci mikroskopů, ale nasazených přímo do akce.
Tisk zevnitř ven: Jak to funguje?
Tradiční metody vyžadovaly, aby buňky „polkly“ částice, což omezovalo možnosti. Nyní vědci vpraví kapku světlocitlivé pryskyřice přímo do cytoplazmy buňky. Tam ji ultrafintní laser selektivně ztvrdí podle předem daného 3D návrhu. Vzniká tak přesná struktura, například malý slon o velikosti pouhých 10 mikrometrů. Zbytek nezpolymerizované pryskyřice se postupně rozpustí, aniž by buňku poškodil.
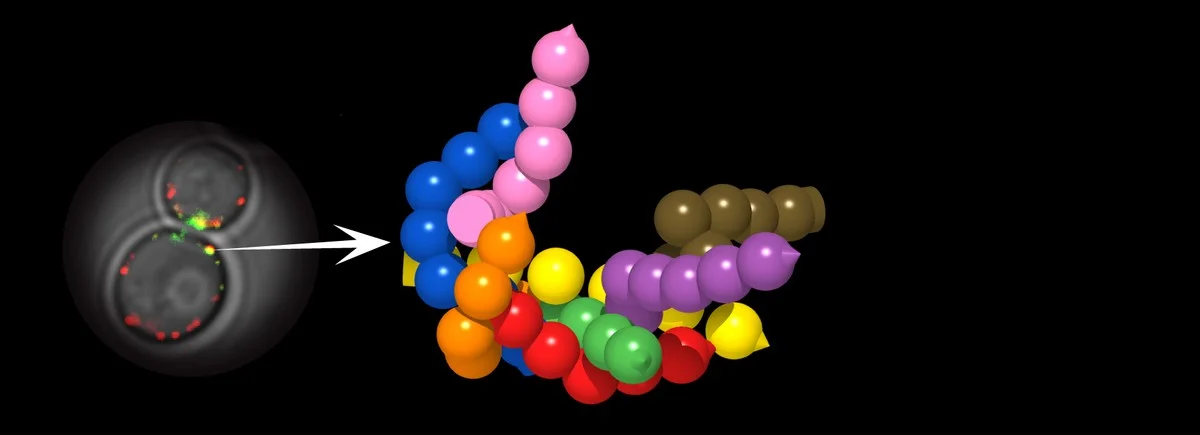
Klíčové je, že buňka tento proces přežije. A nejen to, následně se může i dělit a vytištěnou strukturu předat dceřiným buňkám. To je obrovský posun oproti předchozím technikám.
Od geometrie k optickým zařízením
Pomocí této metody lze vytvořit nejen složité geometrické tvary, ale i miniaturní optické součástky, jako jsou difrakční mřížky, které dokáží promítat světelné vzory v závislosti na orientaci buňky. Vědci dokázali vytisknout dokonce i miniaturní lasery fungující na principu tzv. „whispering gallery mode“ rezonátorů. Tyto malé optické prvky po aktivaci vydávají světlo s jedinečným podpisem.
Představte si, že bychom mohli takto „označit“ jednotlivé buňky pro sledování. Tato technologie umožňuje vytvářet tzv. intracelulární čárové kódy, které mohou nést více dat než je počet buněk v lidském těle.
Testování limitů života a struktury
Samozřejmě, nejsme ještě v situaci, kdy bychom mohli buňkám tisknout čokoládu. Studie ukázaly, že po 24 hodinách přežilo asi 55 % buněk s vytištěnými strukturami. Co je ale důležité, většina úmrtí byla způsobena spíše poškozením membrány během injekce, nikoli samotným tiskem. Některé buňky navíc neztratily svou aktivitu a jedna z nich dokonce prošla dělením a předala svůj interní 3D-tištěný znak jedné ze svých dceřiných buněk.
Buňka se dokázala přizpůsobit. Většina vnitřních komponent, jako je jádro nebo aktinová vlákna, se kolem vytištěných objektů uspořádala bez deformací. To svědčí o vysoké míře integrace.

Praktická hodnota pro budoucnost
Tato technologie má obrovský potenciál pro budoucí medicínu a biologii. Co kdybychom v budoucnu mohli tisknout mechanické páky nebo bariéry uvnitř buněk, které by fyzicky interagovaly s organelami? Nebo bychom mohli vyvinout materiály, které by se rozprostřely po cytoplazmě a umožnily tak kompletní vnitřní ovládání buňky?
I když je technologie zatím ve fázi výzkumu, představte si aplikace v boji proti nemocem, v regenerativní medicíně nebo v přesném cílení léků. Místo aby léky působily plošně, mohli bychom je „naprogramovat“ tak, aby interagovaly s buňkami na molekulární úrovni!
Co myslíte, jaké další nečekané využití by taková technologie mohla mít?